Evaluación de la cascada de cuidados en individuos con VIH/SIDA en un centro ambulatorio de referencia en el Nordeste de Brasil
Geysa Maria Nogueira Farias1, José Reginaldo Pinto2, Geraldo Bezerra da Silva Junior1, Jeová Keny Baima Colares1, Lara Gurgel Fernandes Távora1, Danielle Malta Lima1
1 Universidad de Fortaleza
2 Secretaria de Salud del Estado de Ceará
ABSTRACT
Antecedentes: La cascada constante de tratamiento/cuidados ha emergido como una estrategia a fin de dejar atrás la infección por VIH en busca de la meta última del tratamiento, que es la supresión viral. El estudio apunta a describir la cascada de cuidados en individuos con VIH/SIDA en un Servicio Ambulatorio Especializado.
Métodos: El diseño del estudio es un grupo retrospectivo de individuos adultos con diagnosis confirmada del VIH/SIDA, quienes iniciaron su seguimiento en el Centro de Cuidados Médicos Integrados (NAMI) de la Universidad de Fortaleza (UNIFOR), en la ciudad de Fortaleza, estado de Ceará, en el nordeste de Brasil. Las informaciones siguientes fueron utilizadas en la investigación: CD4+/CD8+ carga viral y carga viral del VIH/SIDA. Los individuos fueron clasificados en dos grupos: retenidos (grupo 1) y no retenidos (grupo 2), totalizando una muestra de 511 participantes. Resultados: El análisis de variable única entre estos grupos demostró que había una predominancia significativa de pacientes masculinos con una edad promedio más elevada en el grupo 1 (p = 0.01). Un antecedente de adicción previa a narcóticos durante la primera consulta fue más frecuente en el segundo grupo (p = 0.001 y p = 0.01 respectivamente). Los pertenecientes al grupo 1, de manera más frecuente, tenían antecedentes de infecciones sexualmente transmitidas (IST) (p = 0.002) y estaban más inmunosuprimidos a la época del diagnóstico (p = 0.002). El uso de TARV (terapia antirretroviral) en la primera consulta fue también más significativo en el grupo de pacientes retenidos (p <0.001). Conclusiones: El estudio sugiere la necesidad de mejorar la “cascada de tratamiento/cuidados” mediante su expansión, a fin de abordar los riesgos de conducta dinámica, lo cual puede transponer las barreras sistémicas de acceso a los servicios de salud para las personas que conviven con VIH/SIDA.
Términos clave: Síndrome de Inmunodeficiencia Adquirida-Terapia Antirretroviral de Elevada Actividad- Cuidados de Salud, Cascada de Cuidados/Tratamiento.
INTRODUCCIÓN
A pesar de los avances científicos y tecnológicos que apuntan al tratamiento y cura de las personas que conviven con VIH/SIDA (PLHA) y las políticas públicas adoptadas por varias naciones y agencias gubernamentales a fin de combatir la enfermedad, el número de individuos infectados que desconocen su estado serológico constituye aun una cuestión de grave preocupación, especialmente en los países en desarrollo, en los cuales la infección se concentra en sus sitios epidémicos [1].
La Organización Mundial de la Salud (OMS) ha denominado poblaciones clave a aquellas definidas como las más vulnerables a la transmisión y diseminación del VIH/SIDA en todo el mundo, agrupando a los hombres que practican sexo con hombres, a las trabajadoras sexuales, a los individuos transgénero, a las personas que hacen uso de drogas ilícitas inyectables y a las poblaciones en reclusión. El Programa Conjunto de las Naciones Unidas sobre VIH/SIDA (ONUSIDA/UNAIDS) estima que 44% de todas las nuevas infecciones por VIH en adultos de todo el mundo se producen entre las poblaciones clave y sus parejas [2,3].
Los individuos con VIH que no adhieren a los cuidados que la infección requiere comprenden un grupo heterogéneo, y consiste en aquellos que nunca alcanzan un cierto nivel de atención, los caracterizados por un proceso longitudinal de compromiso, abandono del mismo y nuevo comprometimiento con la terapia antirretroviral (TARV), así como aquellos completamente ajenos a los cuidados de salud y al sistema de salud [4].
Considerando estos hechos, en 2014, ONUSIDA propuso el establecimiento de metas a fin de maximizar los beneficios individuales y colectivos referidos al diagnóstico y tratamiento de la infección [1]. La cascada constante de cuidados/tratamiento surgió como una estrategia que va desde la infección hasta la meta última del tratamiento, es decir, la supresión viral. Este modelo de tratamiento apunta a involucrar y ayudar a las comunidades médicas para que lideren esfuerzos a fin de lograr, testear, tratar y retener a las poblaciones con la infección clave en los servicios, así como con referencia a la necesidad de abordar las barreras estructurales – incluyendo la estigmatización, discriminación, violencia de género y, en muchos casos, la incriminación [2].
Esta estructura de cascada se tornó conocida como la estrategia 90-90-90, puesto que propone que el diagnóstico y tratamiento del VIH/SIDA se expandirá en 2020 como sigue: 90% de las personas que conviven con VIH/SIDA (PLHAs por sus siglas en inglés) sabrán su condición serológica; de estos, 90% van a utilizar medicaciones para tratar el VIH/SIDA (ART por sus siglas en inglés) y 90% de aquellos en tratamiento conseguirán la supresión viral [1,5,6]. En la representación gráfica de una cascada de tratamiento para VIH/SIDA, el lado izquierdo describe las acciones obtenidas por el tamizaje del VIH/SIDA y el lado derecho brinda la información sobre la eficacia del tratamiento en aquellos que han sido diagnosticados [3]. Varios modelos de cascada se utilizan en todo el mundo. Algunos países utilizan cascadas con cinco barras porque no poseen información de buena calidad para marcar la diferencia entre los vinculados y los retenidos, utilizando solamente el primero de estos. Por otro lado, otros utilizan una séptima barra, “retenidos en ART” (o sea, que utilizan medicación), antes de la barra de supresión viral [5]. El modelo de la cascada brasileña establecido por el Ministerio de Salud consiste en seis pilares, divididos de esta manera: Personas que conviven con VIH/SIDA (PLHAs), personas diagnosticadas, vinculadas al tratamiento, retenidas por causa del tratamiento, utilizando medicaciones para tratar el VIH/SIDA, y con supresión viral [1]. Esta supresión viral permite la reconstitución inmunológica, conduciendo a la suspensión de la enfermedad a largo plazo, y una supervivencia prolongada [7].
En un estudio que evaluó la cascada de cuidados en varios estados brasileños, se observaron fallas en la prevención de la transmisión vertical del VIH/SIDA, independientemente del período en el cual la infección fue diagnosticada en mujeres embarazadas. También se identificó que, en el norte de Brasil, 20% de las mujeres encintas desconocían su situación respecto del VIH/SIDA al momento de dar a luz y 29% ni siquiera habían hecho exámenes durante el período prenatal. De la misma manera que la región del norte, el nordeste brasileño mostró también índices bajos de testeo anti-VIH/SIDA en el período prenatal, respectivamente, 69.9% y 68.4%. Los autores mostraron también que más del 90% de las mujeres embarazadas con VIH/SIDA positivo no utilizaron medicaciones para tratar la infección durante los cuidados prenatales, conduciendo a fallas en la prescripción del tratamiento, incluso entre aquellas que sabían que eran VIH/SIDA positivas.
Otra dificultad identificada fue el desempeño de la sección cesárea electiva y la utilización de medicaciones para tratar VIH/SIDA en los recién nacidos dentro de las primeras 24 horas de vida [8]. En este contexto, puede observarse que la respuesta a la cascada de cuidados debe ir más allá de la disponibilidad de medicinas para el tratamiento del Sida, incluyendo el diagnóstico oportuno, la conexión, la retención (de la infectada) y la estructuración de cuidados en las unidades que brindan cuidados médicos [9].
El objeto del presente estudio consiste en describir la cascada de cuidados en individuos con VIH/SIDA en un Servicio Ambulatorio Especializado en el estado de Ceará, en el nordeste de Brasil.
MÉTODOS
Es el presente un estudio de cohorte retrospectivo de individuos adultos con diagnóstico confirmado de VIH/SIDA que iniciaron su seguimiento/follow-up en el Centro de Cuidados Médicos Integrados (SAE NAMI) de la Universidad de Fortaleza (UNIFOR), en la ciudad de Fortaleza, estado de Ceará, en el nordeste de Brasil. El SAE NAMI fue implementado en Agosto de 2010 y es un centro de tratamiento ambulatorio especializado para pacientes con VIH/SIDA.
Este estudio incluyó participantes que iniciaron su seguimiento desde la implementación del servicio en 2010 hasta diciembre de 2017, registrados en los archivos médicos archivados en el Servicio de Archivo Médico y Estadístico (SAME) de la institución.
Los sujetos de estudio fueron clasificados en dos grupos: individuos que fueron retenidos en cuidados médicos en el SAE NAMI o en otro servicio (con por lo menos dos exámenes de cargas virales del VIH/SIDA o de los exámenes CD4 realizados en el último año o que fueron dispensados de medicaciones para tratar VIH/SIDA en los últimos 100 días del año) e individuos que abandonaron el seguimiento y no fueron retenidos (no llevaron a cabo testes de carga viral y de CD4 durante el último año o durante más de 100 días sin distribución de la medicación propia del VIH/SIDA). La muestra consistió en 511 participantes.
El diagnóstico de infección por VIH siguió las Directrices de Ministerio de Salud [10].
En esta investigación, se analizaron los datos siguientes obtenidos de los registros médicos: variables demográficas (género, edad, origen y nivel de escolaridad); hábitos (adicción al tabaco, consumo de bebidas alcohólicas, uso de drogas ilícitas en los últimos tres meses); datos de conducta (compañeros sexuales durante el año anterior; serología fija del compañero/a, orientación sexual, uso de condones); caracterización de infección por VIH (clasificación de acuerdo a los criterios clínicos y recuento de 1993 de CDC LTCD4, aparición de enfermedades que definen al SIDA); fidelidad al seguimiento/follow-up (tiempo de seguimiento en el servicio, utilización de medicación en el seguimiento (tiempo de seguimiento en el servicio, uso de medicación antirretroviral, antecedentes de medicación antirretroviral, fidelidad al tratamiento); infecciones sexualmente transmitidas, datos de laboratorio (primer LTCD4 y primera carga viral (VL por sus siglas en inglés), LTCD4 y VL antes del primer uso de medicación (ART). LTCD4 y carga viral (VL) antes de la medicación actual y el último LTCD4 disponible y exámenes de carga viral (VL).
El análisis estadístico fue llevado a cabo utilizando SPSS para Windows, versión 23.0 (IBM, EE. UU.). Se calcularon las mediciones de frecuencia y la tendencia central. La prueba Kolmogorov-Smirnov fue utilizada para evaluar la distribución de variables numéricas. Para el análisis comparativo entre los dos grupos, el test por chi cuadrado para variables categóricas y el test de T-Student o de Mann-Whitney fueron utilizados para las variables numéricas, con o sin distribución normal respectivamente. Todas las variables que mostraron diferencia estadística con una significancia <0.2 en el análisis de variable única fueron incluidas en el análisis de regresión logística. Para este análisis, p <0.05 fue considerado como estadísticamente significativo.
Este estudio forma parte de un proyecto denominado CHRONOS que busca evaluar los aspectos epidemiológicos, clínicos y de laboratorio de pacientes con VIH/SIDA tratados en una unidad de salud secundaria, luego de la aprobación del Comité de Ética y de Investigaciones de la Universidad de Fortaleza (UNIFOR) según la Opinión Nº. 957.848 (12/12/2015).
RESULTADOS
El presente estudio incluyó a 511 participantes, de los cuales el 83,4% eran de sexo masculino, 93,9% residían en Fortaleza, y 22,5% poseían título universitario o de educación superior completo o incompleto. Con relación al análisis de vulnerabilidades, 51,1% informaron poseer múltiples compañeros sexuales, 54% eran homosexuales, 26.5% habían tenido relaciones sexuales con individuos VIH positivos. El uso previo de drogas ilícitas fue informado en 27,2% de los casos, siendo la marihuana y la cocaína las drogas usadas más frecuentemente (18,8% y 18% respectivamente).
Más que la mitad de los pacientes (59,9%) poseían antecedentes previos de consumo de bebidas alcohólicas y 36,2% tenían antecedentes previos de uso de tabaco. En 41,1% de los casos, se contaba con un informe de una infección anterior sexualmente transmitida o evidenciada durante la primera consulta, siendo la sífilis la más prevalente (24,9%), seguida por la uretritis (8,8%) y condiloma (8,2%) (Tabla 1).
Tabla 1. Distribución del perfil epidemiológico clínico de pacientes con VIH/SIDA tratados en el NAMI, Fortaleza, Ceará, Brasil, 2010 to 2017.
|
Variables Evaluadas |
Resultado |
|
Variables Demográficas |
|
|
Género Femenino |
426 (83,4%) 85 (16,6%) |
|
Origen Fortaleza Otros |
480 (93,9%) 31 (6,1%) |
|
Nivel de escolaridad Analfabetos Alfabetizados No terminaron la escolaridad primaria Terminaron la escolaridad primaria Finalizaron/No finalizaron educación secundaria Finalizaron/No finalizaron Educación terciaria/Universidad Desconocido |
9 (1,8%) 6 (1,2%) 73 (14,3%) 23 (4,5%) 271 (53%) 115 (22,5%) 14 (2,7%) |
|
Promedio de edad en años (diferencia estándar) |
33,4 (+/-10,6) |
|
Variables de vulnerabilidad |
|
|
Número de compañeros Fijos Múltiple Sin compañero Desconocido |
213 (41,7%) 261 (51,1%) 31 (6,1%) 6 (1,2%) |
|
Orientación Sexual Homosexual Bisexual Heterosexual Desconocido |
276 (54%) 52 (10,2%) 162 (31,7%) 21 (4,1%) |
|
Práctica de sexo con individuos VIH + |
134 (26,5%) |
|
Antecedentes de transfusión sanguínea |
24 (4,7%) |
|
Adicción previa a drogas ilícitas |
139 (27,2%) |
|
Adicción a drogas ilícitas a la época de la 1a. Consulta |
71 (13,9%) |
|
Antecedentes de consumo de bebidas alcohólicas |
306 (59,9%) |
|
Consumo de bebidas alcohólicas a la época de la 1a. consulta |
265 (51,9%) |
|
Antecedentes de adicción al tabaco |
185 (36,2%) |
|
Tabaquismo al tiempo de la 1a. consulta |
112 (21,9%) |
|
Antecedentes de Enfermedades Sexualmente Transmitidas |
210 (41,1%) |
|
Número de Enf. Sex. Transmitidas 1 2 3 |
177 (34,6%) 25 (4,9%) 7 (1,4%) |
|
Variables Clínicas |
|
|
Presencia de comorbilidades en la 1a. consulta |
286 (56%) |
|
Casos de enfermedades definidoras de VIH en la 1a. consulta |
53 (10,4%) |
|
Número de enfermedades definidores de VIH 1 2 3 4 |
41 (8%) 9 (1,8%) 3 (0,6%) 1 (0,2%) |
|
Clasificación CDC según síntomas al diagnóstico: A B C Desconocido |
282 (55,2%) 165 (32,3%) 53 (10,4%) 11 (2,2%) |
|
Clasificación CDC según niveles de CD4 al diagnóstico 1 2 3 Desconocido |
178 (34,8%) 174 (34,1%) 105 (20,5%) 54 (10,6%) |
|
Media/Promedio 1er nivel producido CD4 |
432 céls/dL (+/- 279) |
|
Media 1a carga viral producida |
3,57 log (+/- 1,5) |
|
Uso de medicación antirretroviral a la 1a. consulta |
257 (50,3%) |
|
NADIR CD4 |
388 céls/dL (+/- 271) |
|
Media carga viral antes de medicación Antirretroviral 1 |
4,1log (+/- 1,09) |
|
TOTAL |
511 (100%) |
Clínicamente, 56% poseía alguna comorbilidad en la primera consulta, siendo la hipertrigriliceridemia la más prevalente (17%). En la primera consulta, 10,4% poseía un diagnóstico actual o confirmado previamente de alguna enfermedad definidora del SIDA. Entre las que fueron identificadas más frecuentemente se encontraban: candidiasis esofágica, en 20 (26%), neumocistosis en 15 (19%), tuberculosis extrapulmonar en 13 (18%), y neurotoxoplasmosis en 11 (15%). Con relación a la clasificación del CDC al tiempo del diagnóstico, 55,2% pertenecían al grupo A (asintomáticos) y 34,8% al grupo 1 (LTCD4 >500 células / dL). Aproximadamente la mitad de los pacientes (50,3%) estaban recibiendo medicación para VIH/SIDA en la primera consulta y los parámetros de laboratorio mostraban que el promedio del primer test LTCD4 realizado era de 432 células/dL (+/- 279), estando aun ligeramente arriba del nadir LTCD4, que era de 288 células / dL, mientras que el primer promedio de carga viral del VIH fue de 3.571log (+/- 1.5), tal como demostrado en la Tabla 1.
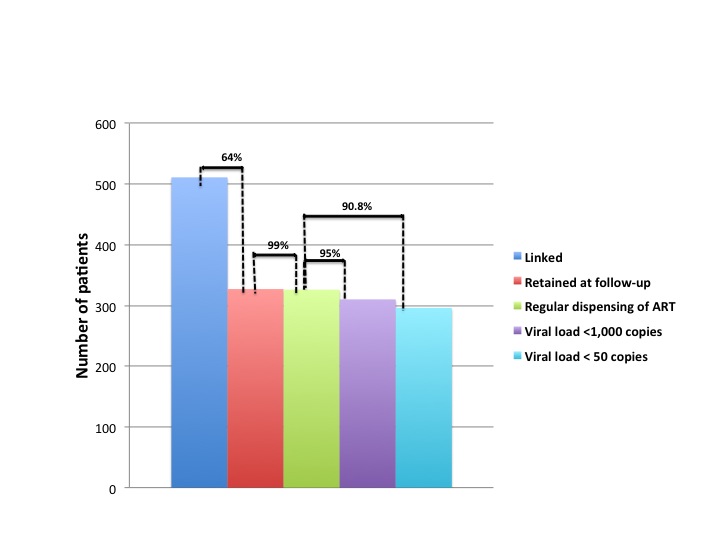
El análisis de retención en el servicio mostró que 63,8% de los pacientes estaban concurriendo al servicio ambulatorio y que estaban recibiendo medicación para el VIH/SIDA regularmente, que era ofrecida por la farmacia; 0,2% hacían un seguimiento regular, pero se demoraba la entrega de la medicación antirretroviral en la farmacia- 5,7% había abandonado las consultas pero estaban al día con la medicación antirretroviral brindada por las farmacias; y 30,3% había abandonado totalmente el tratamiento. El promedio de duración del seguimiento/follow-up era de 39 meses, y 8,4% de los pacientes había acudido solamente a una consulta. La mayoría de los pacientes (71,6%) había comenzado a ingerir la medicación antirretroviral con regímenes conteniendo la combinación de 2 inhibidores análogos nucleósidos de transcriptasa reversa y 1 no análogo, y 46,8% de los pacientes estaban aún utilizando el primer régimen antirretroviral. Esta asociación era también la prescrita con mayor frecuencia en la medicación antirretroviral en la última consulta (65%), en cuya oportunidad 84,7% de los pacientes estaban siguiendo el tratamiento. De éstos, 76,3% reportaron continuidad con la medicación antirretroviral. El análisis de respuesta a la medicación antirretroviral mostró que, incluso luego de incluir a los pacientes que habían abandonado el tratamiento, la carga viral se situaba por debajo de las 50 copias/dL (71.5%) y por debajo de las 1.000 copias/dL (94%) en un número considerable de pacientes.
La Figura 1 muestra la cascada de cuidados/tratamiento para pacientes con VIH/SIDA. Puede observarse que, aunque existe una pérdida considerable de conexión (64% estaban aún retenidos en el servicio), 99% de los pacientes retenidos reciben regularmente la medicación a través de la farmacia. De estos últimos, 95% tuvieron el último VL <1000 copias / dL y 90.8% <50 copias / dL.
Figura 1. Cascada de cuidados/tratamientos de pacientes con VIH/SIDA, tratados en el NAMI, Fortaleza, Ceará, Brasil, 2010-2017.

Figura 2: Flujograma de pacientes que abandonaron el tratamiento de la VIH/SIDA en el NAMI, Fortaleza, Ceará, Brasil, 2010-2017.
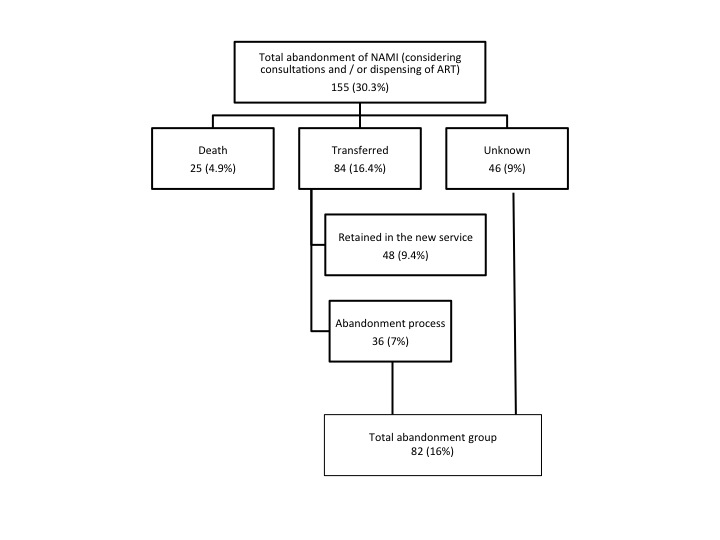
De los 25 pacientes que fallecieron, solamente 3 dejaron de existir a raíz de causas no relacionadas con VIH – meningococemia, muerte por ahorcamiento (suicidio) y lesiones por armas de fuego.
Luego de la exclusión de estas 25 muertes, los pacientes fueron entonces clasificados en dos grupos, con el grupo 1 consistiendo en pacientes retenidos para seguimiento en el SAE NAMI o en otro servicio y el grupo 2 comprendiendo a los pacientes que habían abandonado totalmente el tratamiento, o aquellos cuya condición de seguimiento/follow-up era desconocido (Figura 2). El análisis de variable única entre estos grupos demostró que había una predominancia significativa de pacientes del sexo masculino, con una edad promedio más avanzada en el grupo 1 1 (p = 0.01). Un historial de adicción previa a las drogas y durante la primera consulta fue más frecuente en el grupo 2 (p = 0.001 y p = 0.01 respectivamente). Los pacientes en el grupo 1 presentaban antecedentes de infecciones de transmisión sexual (ITS) con mayor frecuencia (p = 0.002) y fueron más inmunosuprimidos al tiempo del diagnóstico (p = 0.002). El uso de medicación antirretroviral en la primera consulta fue también más significativo en el grupo de pacientes retenidos (p <0.001) (Tabla 2).
Tabla 2. Análisis de variable única entre pacientes con VIH/SIDA retenidos y no retenidos que pasan por seguimiento ambulatorio en el NAMI, Fortaleza, Ceará, Brasil, 2010-2017.
|
Variables evaluadas |
Grupo 1 |
Grupo 2 |
p |
|
Variables demográficas |
|||
|
Género Masculino Femenino |
344 (85,1%) 60 (14,9%) |
61(74,4%) 21 (25,6%) |
0.01 |
|
Nivel de escolaridad Analfabeto Alfabetizado No finalizó educación primaria Finalizó educación primaria Finalizó/no finalizó educación secundaria Finalizó/no finalizó educac. terciaria/universitaria Desconocido |
6 (1,5%) 3 (0,7%) 54 (13,4%) 18 (4,5%) 212 (52,5%) 99 (24,5%) 12 (3%) |
2 (2,4%) 1 (1,2%) 13 (15,9%) 5 (6,1%) 46 (56,1%) 13 (15,9%) 2 (2,4%) |
0,71 |
|
Edad promedio en años (diferencia estándar) |
34 (+/-10,6) |
30,1 (+/-9,0) |
0,01 |
|
Variables de Vulnerabilidad |
|||
|
Nº de compañeros Fijo Múltiple Sin compañero Desconocido |
178 (44,1%) 198 (49%) 24 (5,9%) 4 (1,0%) |
32 (39%) 46 (56,1%) 3 (3,7%) 1 (1,2%) |
0,83 |
|
Orientación Sexual Homosexual Bisexual Heterosexual Desconocido |
224 (55,4%) 39 (9,7%) 126 (31,2%) 15 (3,7%) |
40 (48,8%) 12 (14,6%) 27 (32,9%) 3 (3,7%) |
0,49 |
|
Práctica de sexo con individuos VIH + |
106 (26,2%) |
22 (26,8%) |
0,98 |
|
Adicción previa a drogas ilícitas |
96 (23,8%) |
34 (41,5%) |
0,001 |
|
Adicción a drogas ilícitas al tiempo de la 1a. consulta |
47 (11,6%) |
18 (22%) |
0,01 |
|
Antecedentes de consumo de bebidas alcohólicas |
246 (60,9%) |
49 (59,8%) |
0,53 |
|
Consumo de bebidas alcohólicas a la época de la 1a. consulta |
211 (52,2%) |
46 (56,1%) |
0,06 |
|
Antecedentes de adicción al tabaco |
139 (34,4%) |
36 (43,9%) |
0,89 |
|
Tabaquismo al tiempo de la 1a. consulta |
77 (19,1%) |
28 (34,1%) |
0,27 |
|
Antecedentes de Enfermedades Sexualmente Transmitidas |
182 (45%) |
22 (26,8%) |
0,002 |
|
Variables clínicas |
|||
|
Presencia de comorbilidades a la 1a. consulta |
228 (56,4%) |
41 (50%) |
0,28 |
|
Casos de enfermedades definidoras de VIH a la 1a. consulta |
42 (10,4%) |
6 (7,3%) |
0,39 |
|
Clasificación CDC según síntomas al tiempo del diagnóstico A B C Desconocido |
232 (57,4%) 122 (30,2%) 43 (10,6%) 7 (1,7%) |
40 (48,8%) 33 (40,2%) 6 (7,3%) 3 (3,7%) |
0,25 |
|
Clasificación CDC según el CD4 al tiempo del diagnóstico 1 2 3 Desconocido |
140 (34,7%) 152 (37,6%) 79 (19,6%) 33 (8,2%) |
34 (41,5%) 18 (22%) 14 (17,1%) 16 (19,5%) |
0,002 |
|
Media/Promedio 1er nivel producido CD4 |
431,8 céls. /dL (+/- 279) |
486,4 céls/dL (+/- 287) |
0,15 |
|
Media 1a carga viral producida |
3,12 log (+/- 1,5) |
3,0 log (+/- 1,4) |
0,62 |
|
Uso de medicación antirretroviral a la 1a. consulta |
222 (55%) |
25 (30,5%) |
<0,001 |
|
NADIR CD4 |
401 céls/dL (+/- 280) |
346 céls/dL (+/- 214) |
0,38 |
|
Media carga viral antes de medicación Antirretroviral 1 |
3,67 log (+/- 1,0) |
3,60 log (+/- 0,96) |
0,49 |
|
TOTAL |
404 |
82 |
|
El análisis de regresión logística, sin embargo, mostró una diferencia estadísticamente significativa entre los dos grupos relativa solamente a las variables de adicción previa a las drogas (p = 0.02), historia de ITS (p = 0.008), clasificación CDC por LTCD4 al tiempo del diagnóstico (p = 0.007) y uso de medicación antirretroviral en la primera consulta (p <0.001).
DISCUSIÓN
Con relación a los datos sociodemográficos, la mayoría de los pacientes eran individuos jóvenes del sexo masculino, con estudios secundarios o de nivel educacional más elevado. Con relación a este hecho, el último boletín epidemiológico del Ministerio de Salud, en el año 2018, demostró que 65,2% de las personas que conviven con VIH/SIDA se situaban en el grupo de edad de los 20-39 años, 29.4% había finalizado la educación secundaria, siendo la mayoría de sexo masculino [11].
Esta predominancia de infección por VIH en pacientes hombres puede también verse en otras poblaciones. Estudios realizados en Turquía y regiones fuera del África Subsahariana encontraron resultados similares. Estos investigadores consideran que la incidencia más elevada entre hombres jóvenes se debe, en parte, a su conducta de alto riesgo en términos de transmisión, tal como contacto con prostitutas y homosexualidad [12,13].
La evaluación de las costumbres, en este estudio, mostró que la mayoría de los individuos eran homosexuales, seguidos por heterosexuales; un porcentaje significativo de usuarios de drogas y antecedentes de adicción a las bebidas alcohólicas y enfermedades transmitidas sexualmente.
La población clave con riesgo elevado de contraer VIH ha avanzado desde los usuarios de drogas y trabajadores sexuales al público en general. El VIH se ha convertido en una seria amenaza a la salud pública y un importante factor limitador de la estabilidad social y del desarrollo económico [14].
Se estima que más de un millón de individuos conviven actualmente con VIH en los EE. UU. y muchos de ellos poseen adicción crónica al alcohol. Los índices de abuso de bebidas alcohólicas se reportan en el orden del 40 al 50% de los pacientes evaluados. El abuso del alcohol y de las drogas ilícitas son indicadores significativos de falta de fidelidad al uso de medicación antirretroviral. Las personas que tienen VIH/SIDA que sufren de desórdenes causados por el uso de bebidas alcohólicas y de drogas son consideradas de manera consistente como no adeptos a la ingestión de medicación antirretroviral y tienen una probabilidad más elevada de falta de supresión virológica y de consecuencias adversas a causa de la enfermedad. A medida que la infección por VIH se ha tornado en enfermedad con un curso más crónico, las condiciones de comorbilidad pueden alterar el curso de la dolencia, afectando la función metabólica. El uso y abuso de drogas ilícitas es fuertemente desalentado en esta población de pacientes [15,16]. El uso de alcohol en pacientes con VIH puede causar senescencia inmunológica (los efectos del envejecimiento de la función del sistema inmunológico), inflamación e hipercoagulabilidad [16,17]. Dicha prevalencia elevada en esta población constituye una cuestión seria y curiosa al mismo tiempo, dado que la infección viral y el consumo de bebidas alcohólicas interactúan de alguna manera para incrementar sus efectos dañinos [18]. El uso de bebidas alcohólicas posee una asociación fuerte y consistente con la incidencia del VIH. Las asociaciones entre el uso del alcohol y las conductas sexuales riesgosas han sido identificadas de manera consistente. Los usuarios de bebidas alcohólicas poseen intenciones más fuertes de practicar sexo sin protección, con comunicación sexual y habilidades de negociación más pobres, así como de niveles más elevados de excitación sexual y, consecuentemente, de transmisión por VIH [16].
Los hombres que practican sexo con hombres se ven también desproporcionadamente afectados por el VIH y por otras infecciones transmitidas sexualmente (ITS). El hecho de ser diagnosticado con una ITS se sitúa entre los factores de riesgo más consistentes y duraderos asociadas al contagio por VIH. El alto riesgo de contraer el VIH entre las ITS bacterianas refleja alguna combinación de susceptibilidad aumentada, conductas de riesgo sostenidas y factores de redes sexuales [19].
La asociación entre el contagio del VIH y las enfermedades transmitidas sexualmente constituye una cuestión compleja y multidireccional. Cierta evidencia sugiere que la inflamación del tracto genital causada por las enfermedades transmitidas sexualmente aumenta el riesgo de transmisión del VIH por medio del aumento de compañeros infectados por el VIH y debido a lesiones en el epitelio del tracto genital y el reclutamiento de células objetivo para esta área en individuos/compañeros susceptibles al VIH. Las infecciones del recto constituyen marcadores directos de sexo anal receptivo inseguro, que se asocia a un mayor riesgo de contraer VIH. También, debido a que la epidemia de sífilis en los EE. UU. y en otros países desarrollados se concentra entre personas del sexo masculino que practican sexo entre ellas y conviven con VIH, la sífilis precoz puede ser un marcador de sexo sin protección dentro de las redes sexuales, incluyendo el elevado riesgo de los compañeros sexuales con VIH. [19,20].
Más de la mitad de la muestra en el presente Estudio tenía algún tipo de comorbilidad, pero solamente una pequeña porción poseía alguna enfermedad definitoria del SIDA.
Las comorbilidades pueden complicar y acelerar el proceso de la enfermedad de VIH, manifestando su fragilidad, deficiencia en órganos y funciones y posibilidad incrementada de hospitalización y muerte. La prevalencia en aumento de las comorbilidades puede afectar la gestión clínica de los pacientes con VIH/SIDA. Estas comorbilidades pueden interferir con la iniciación de la medicación a base de antirretrovirales, interrumpir el metabolismo de los mismos, o exigir terapia con drogas que pueden interferir con la medicación antirretroviral, complicando el tratamiento y la supervivencia de los pacientes con VIH/SIDA. Las comorbilidades tales como la enfermedad arterial coronaria, la diabetes mellitus, hipertensión, dislipidemia, enfermedad ósea, del hígado o riñones, desórdenes respiratorios crónicos, cáncer y condiciones neurocognitivas y siquiátricas constituyen ejemplos de complicaciones severas que interfieren con el tratamiento de la infección [21,22,23].
Un estudio llevado a cabo en Malasia ha demostrado que las comorbilidades encontradas más comúnmente en pacientes con VIH/SIDA fueron las enfermedades infecciosas, tales como la hepatitis C, tuberculosis, herpes simplex, candidiasis y otras infecciones oportunistas. Las coinfecciones de tuberculosis pueden empeorar la calidad de vida de los pacientes infectados con VIH [23].
Estudios llevados a cabo en otros países en desarrollo han reportado índices elevados de mortalidad en pacientes hospitalizados con VIH, cuando comparados con los países desarrollados (hasta el 38% versus 2,6%). La mortalidad se asocia a las etapas avanzadas de la enfermedad, la severidad de la disfunción inmunológica (bajo recuento de CD4), presencia de infecciones oportunistas y falta de recursos para el tratamiento o cuidados [24].
En nuestra muestra, la mayoría de los casos de fallecimiento se relacionaban aún con la evolución de la infección por VIH. Históricamente, el desarrollo de la medicación antirretroviral redujo de forma dramática los costos de hospitalización, reduciendo los índices de hospitalización. Es más probable que las personas que conviven con VIH/ SIDA fallezcan a raíz de otras enfermedades y no debido al SIDA [22,23]. Las diferencias en acceso a programas, suministro de medicación y un diagnóstico oportuno han demostrado ejercer influencia en los resultados para los pacientes [24].
Aunque más del 60% de los pacientes tuvieron un buen seguimiento y fueron retenidos en el servicio, un porcentaje significativo (más del 30%) se perdió en el tema del seguimiento en el SAE NAMI. Si uno considera que 48 pacientes (9.4%) estaban siendo monitoreados en otro servicio, se puede decir que el índice de retención por seguimiento fue de 73,4%, el cual se sitúa aun por debajo de la meta recomendada por la Organización Mundial de la Salud, que es del 90%. Aun así, es tema de preocupación que 16% de los casos fueran clasificados como de total abandono del seguimiento.
Estudios llevados a cabo en Brasil indican consumo de bebidas alcohólicas, uso de drogas ilícitas, ingreso familiar bajo, nivel educativo bajo, la presencia de enfermedades psiquiátricas y un intervalo de 1 a 3 años entre el diagnóstico de positividad del VIH y el inicio de la ingestión de medicación antirretroviral como factores relacionados a la falta de fidelidad al tratamiento [25]. Estudios previos han identificado que las creencias relativas al VIH, el estigma asociado al conocimiento del estado respecto del VIH, los costos de alimentos y de transporte, el uso de sustancias, la carga de píldoras, los eventos adversos por drogas y la falta de comunicación con los profesionales de salud constituyen factores asociados a la falta de fidelidad al programa de ingestión de medicamentos antirretrovirales [26].
Aunque alcanzamos porcentajes >90% en todo el rango de cascadas, salvo para el cambio del primero al segundo, resulta claro que aun tenemos que mejorar la retención de esos pacientes. Las mejoras en los indicadores de cascada con el transcurso del tiempo se deben probablemente a una combinación de factores, tales como el acceso mejorado a cuidados y acceso a medicación antirretroviral, disponibilidad de regímenes de tratamiento que son más efectivos y más fáciles de seguir, cambios en las directrices, recomendación de inicio temprano del tratamiento e interrupciones opuestas a tratamiento, el éxito de las iniciativas de tratamiento y cuidados y/o cambios en la población diagnosticada con el transcurso del tiempo [4,6,27].
El análisis de los factores asociados con la retención o no retención del seguimiento en el NAMI mostró que aquellos que mantuvieron un seguimiento adecuado fueron los de más edad (promedio de 34 años x 30 años), con una frecuencia más baja de adicción a las drogas (23 x 41%), mayor frecuencia de infecciones sexualmente transmitidas (45 x 26%) y frecuencia más elevada de uso de medicación antirretroviral a la primera consulta (55 x 30%).
Con relación a la edad, puede presumirse que los pacientes de más edad muestran un mayor compromiso con su tratamiento o que incluso cuentan con cuidadores, lo que de alguna manera aumenta la fidelidad al tratamiento. La adicción a las drogas constituye un factor de riesgo conocido con relación a la falta de fidelidad al tratamiento en varios ambientes clínicos, [15]. La presencia de enfermedades sexualmente transmitidas puede constituir un factor que conduzca al paciente a buscar el servicio de salud y a permanecer en el seguimiento debido a la presencia de síntomas; es decir, los pacientes asintomáticos son probablemente más descuidados con su tratamiento o pueden no importarse mucho con el hecho de ser VIH positivos, sin darse cuenta de la severidad de la infección. El uso de medicación antirretroviral a la época de la primera consulta puede conducir a una fidelidad para con el tratamiento, dado que los pacientes reciben toda la atención del equipo multidisciplinario, brindándoles una sensación de sentirse cuidados y abrazados por el servicio, haciéndolos desear retornar a las consultas siguientes.
A pesar de la disponibilidad de medicación antirretroviral efectiva, muchas personas que conviven con VIH/SIDA no alcanzan la supresión viral, contribuyendo a la morbilidad y mortalidad por SIDA o no, y a la transmisión subsecuente del VIH. Existen limitadas intervenciones basadas en la evidencia para mejorar la retención en lo que hace al tratamiento. La mayoría de las intervenciones objetivadas pueden mejorar los resultados en las poblaciones altamente vulnerables [28].
La educación sexual en los grupos vulnerables es también otra estrategia para modificar la cascada de cuidados entre pacientes en las instalaciones ambulatorias de pacientes. Mayores desafíos en la negociación relativa al uso de preservativos y nuevos enfoques con relación al riesgo parecen favorecer cambios significativos en la calidad de vida de los pacientes con VIH [29].
Una importante limitación del estudio se asocia al hecho de que la muestra de pacientes estaba principalmente concentrada en Fortaleza, y no puede verificarse si los datos sociodemográficos, culturales y de conducta son similares a aquellos de otras regiones del espacio geográfico verificado. Las comparaciones entre las diferentes unidades de cuidados, sean públicas o privadas, en Ceará, resultarían necesarias a fin de verificar si los resultados del estudio serían similares, dado que la cascada de tratamiento/cuidados no está, aun, completamente distribuida en el interior del estado, de manera que la población pueda contar con acceso igualitario a los servicios, tal como en el escenario propuesto de la investigación.
CONCLUSIONES
El presente estudio sugiere la necesidad de mejorar la “cascada de cuidados/tratamiento” mediante su expansión a fin de abordar riesgos dinámicos de conducta que pueden transponer las barreras sistémicas de acceso a personas que conviven con VIH/SIDA, expandiendo la red de servicios y mejorando la capacidad de retención de los pacientes bajo seguimiento.
Una cascada de cuidados integrados que incorpore experiencias de la evolución de la vida y busque superar los desafíos psicosociales y a nivel de la comunidad, alineados a un modelo combinado de prevención y promoción de la salud puede mejorar de manera más efectiva la salud sexual y psicológica de los pacientes.
AGRADECIMIENTOS
Desearíamos agradecer al Núcleo de Atención Médica Integrada (NAMI) de la UNIFOR, Ceará, Brasil, por su excelente labor de cuidado de los individuos que conviven con VIH/SIDA y la disponibilidad de datos oficiales sobre el tratamiento de estos pacientes para este estudio.
REFERENCIAS
Miranda WA et al. Modelo preditivo de retenção no cuidado especializado em HIV/aids. Cad Saúde Pública. 2018; 34(10): e00209416.
Wolf RC, Bingham T, Millett G, Wilcher R. Building the evidence base to optimize the impact of key population programming across the HIV cascade. J Int AIDS Soc. 2018 Jul;21 Suppl 5:e25146.
Kowalska JD, Ankiersztejn-Bartczak M, Shepherd L, Mocroft A.. Cascade of care and factors associated with virological suppression among HIV-positive persons linked to care in the Test and Keep in Care (TAK) project. Infection. 2018 Aug;46(4):533-540.
Krebs E et al. Informing targeted interventions to optimize the cascade of HIV care using cluster analyses of health resource use among people living with HIV/AIDS. AIDS Behav. 2018 Jan;22(1):234-244.
Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Vigilância, Prevenção e Controle das Infecções Sexualmente Transmissíveis, do HIV/Aids e das Hepatites Virais. Manual Técnico de Elaboração da Cascata de Cuidado Contínuo do HIV. Brasília: Ministério da Saúde, 2017.
Wilton J et al. Trends in HIV care cascade engagement among diagnosed people living with HIV in Ontario, Canada: A retrospective, population-based cohort study. PLoS One 2019 Jan 4;14(1):e0210096.
Nosyk B et al. The cascade of HIV care in British Columbia, Canada, 1996– 2011: a population-based retrospective cohort study. Lancet Infect Dis. 2014 Jan;14(1):40-49.
Miranda AE et al. Avaliação da cascata de cuidado na prevenção da transmissão vertical do HIV no Brasil. Cad. Saúde Pública. 2016; 32( 9 ): e00118215.
Vourli G et al. HIV cascade of care in Greece: Useful insights from additional stages. PLoS One. 2018 Nov 15;13(11):e0207355.
Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Coordenação-Geral da Epidemiologia em Serviços. Guia de vigilância em saúde: volume único. 2ª ed. Brasília: Ministério da Saúde, 2017.
Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de Vigilância, Prevenção e Controle das Infecções Sexualmente Transmissíveis, do HIV/Aids e das Hepatites Virais (DIAHV). Boletim Epidemiológico HIV/AIDS 2018. Brasília, Ministério da Saúde, v. 49, n. 53, 2018.
Ertunc B, Kaya S, Koksal I. Clinico-Epidemiological Analysis of HIV/AIDS Patients. Eurasian J Med. 2016 Oct;48(3):157-161.
Oliveira RC et al. Scientific Production about the Adherence to Antiretroviral Therapy. Int Arch Med. 2017;10:244. doi: 10.3823/2514
Li JZ et al. The Size of the Expressed HIV Reservoir Predicts Timing of Viral Rebound after Treatment Interruption. AIDS. 2016 Jan 28;30(3):343-53.
Molina PE, Amedee AM, Winsauer P, Nelson S, Bagby G, Simon L. Behavioral, Metabolic, and Immune Consequences of Chronic Alcohol or Cannabinoids on HIV/AIDs: Studies in the Non-Human Primate SIV Model. J Neuroimmune Pharmacol. 2015 Jun;10(2):217-32.
Williams EC et al. Alcohol Use and Human Immunodeficiency Virus (HIV) Infection: Current Knowledge, Implications, and Future Directions. Alcohol Clin Exp Res. 2016 Oct;40(10):2056-2072.
Thangavel S et al. Oxidative Stress in HIV Infection and Alcohol Use: Role of Redox Signals in Modulation of Lipid Rafts and ATP-Binding Cassette Transporters. Antioxid Redox Signal 2018 Feb 1;28(4):324-337.
WingO T, Nesil T, Chang SL, Li MD. Interactive Effects of Ethanol and HIV-1 Proteins on Novelty-Seeking Behaviors and Addiction-Related Gene Expression. Alcohol Clin Exp Res 2016 Oct;40(10):2102-2113.
Katz DA, Dombrowski JC, Bell TR, Kerani RP, Golden MR. HIV Incidence among Men Who Have Sex with Men Following Diagnosis with Sexually Transmitted Infections. Sex Transm Dis. 2016 Apr;43(4):249-54.
Kahle EM et al. Sexually Transmitted Disease Testing and Uptake of Human Papillomavirus Vaccine in a Large Online Survey of US Men Who Have Sex With Men at Risk for HIV Infection, 2012. Sex Transm Dis. 2017 Jan;44(1):62-66..
Abara WE, Smith L, Zhang S, Fairchild AJ, Heiman HJ, Rust G. The influence of race and comorbidity on the timely initiation of antiretroviral therapy among older persons living with HIV/AIDS. Am J Public Health. 2014 Nov;104(11):e135-41.
Zingmond DS, Arfer KB, Gildner JL, Leibowitz AA. The cost of comorbidities in treatment for HIV/AIDS in California. PLoS One. 2017 Dec 14;12(12):e0189392.
Nlooto M. Comorbidities of HIV infection and health care seeking behavior among HIV infected patients attending public sector healthcare facilities in KwaZulu-Natal: A cross sectional study. PLoS One. 2017; 12(2): e0170983.
Álvarez Barreneche MF et al. Hospitalization causes and outcomes in HIV patients in the late antiretroviral era in Colombia. AIDS Res Ther 2017 Nov 13;14(1):60.
Silva JAG et al. Fatores associados à não adesão aos antirretrovirais em adultos com AIDS nos seis primeiros meses da terapia em Salvador, Bahia, Brasil. Cad. Saúde Pública. 2015 ; 31(6): 1188-1198.
Webb Mazinyo E et al. Adherence to Concurrent Tuberculosis Treatment and Antiretroviral Treatment among Co-Infected Persons in South Africa, 2008–2010. PLoS One. 2016 Jul 21;11(7):e0159317.
Auld AF et al. Retention Throughout the HIV Care and Treatment Cascade: From Diagnosis to Antiretroviral Treatment of Adults and Children Living with HIV-Haiti, 1985–2015. Am J Trop Med Hyg. 2017 Oct;97(4_Suppl):57-70.
Meade CM, Badell M, Hackett S, et al. HIV Care Continuum among Postpartum Women Living with HIV in Atlanta. Infect Dis Obstet Gynecol. 2019;e8161495. https://doi.org/10.1155/2019/8161495.
Newman PA, Guta A, Lacombe-Duncan A, Tepjan S. Clinical exigencies, psychosocial realities: negotiating HIV pre-exposure prophylaxis beyond the cascade among gay, bisexual and other men who have sex with men in Canada. J Int AIDS Soc. 2018 Nov;21(11):e25211.
Recibido: 28/08/2019
Revisado: 08/05/2020
Aprobado:08/05/2020